ما الذي يجعل المعادن متعددة الاستخدامات ولا غنى عنها في الهندسة؟ يستكشف هذا المقال الأساسيات الأساسية لتبلور الفلزات وبنيتها وتحولاتها. اكتشف كيف تنتقل الفلزات من الحالة السائلة إلى الحالة الصلبة، وأهمية العيوب البلورية، والظواهر الرائعة للتبريد الفائق. من خلال فهم هذه المبادئ، ستكتسب نظرة ثاقبة على خصائص المعادن وتطبيقاتها في مختلف الصناعات.
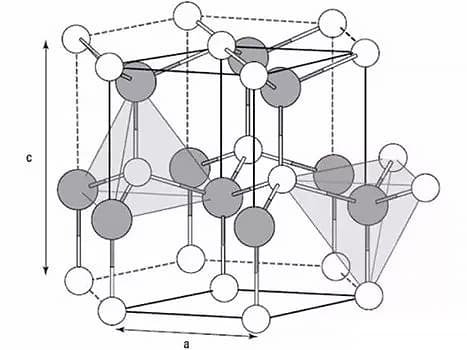
المعادن هي بلورات الحالة الصلبة.
يرتبط التركيب البلوري بالخصائص والتشوه اللدن والتحولات الطورية للمعالجة الحرارية للمعادن.
والشبكات الثلاث الأكثر شيوعًا في الفلزات هي الشبكة المكعبة المتمركزة حول الجسم، والشبكة المكعبة المتمركزة حول الوجه، والشبكة السداسية المتقاربة.
يمكن تصنيف العيوب البلورية إلى ثلاث فئات بناءً على أشكالها الهندسية: العيوب النقطية، والعيوب الخطية، والعيوب المستوية.
تُعرف العملية التي ينتقل بها الفلز من الحالة السائلة إلى الحالة الصلبة (البلورية) باسم تبلور الفلز.
(1) منحنى التبريد وظاهرة التبريد الفائق
منحنى التبريد هو رسم بياني يعرض العلاقة بين درجة الحرارة والزمن أثناء عملية تبريد المادة. يمكن تحديد منحنى تبريد بلورة معدنية باستخدام طرق التحليل الحراري. وتتضمن العملية صهر المعدن للوصول إلى درجة حرارة موحدة قدر الإمكان، وتبريده بسرعة محددة، وتسجيل تغيرات درجة الحرارة بمرور الوقت، ورسم البيانات على رسم بياني لدرجة الحرارة مقابل الزمن للحصول على منحنى التبريد، كما هو موضح في الشكل 1.
تعوض الحرارة الكامنة للتبلور المنطلقة أثناء التبلور الفقد الحراري من المعدن إلى الخارج، مما يتسبب في ظهور خط أفقي على منحنى التبريد. درجة الحرارة المقابلة لهذا الخط هي درجة حرارة التبلور الفعلية للمعدن.
تُظهر التجارب أن درجة حرارة التبلور الفعلية (T1) للمعدن تكون دائمًا أقل من درجة حرارة التبلور النظرية (T0). ويشار إلى هذه الظاهرة باسم التبريد الفائق. ويُعد التبريد الفائق شرطًا لحدوث التبلور. ويُعرف الفرق بين T0 وT1، △T = T0 - T1، بدرجة التبريد الفائق.
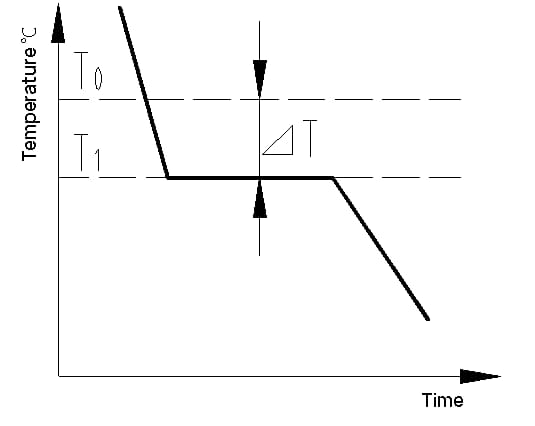
الشكل 1 منحنى تبريد بلورة الحديد النقي
(2) عملية التبلور
تنطوي عملية التبلور على تكوين النوى وتمددها. وتعرف هذه العملية باسم التنوي والنمو.
تُعرف الظاهرة التي يتحول فيها الفلز من بنية شبكية إلى أخرى مع تغير درجة الحرارة في الحالة الصلبة باسم التحول المتساوي الشكل.
بعض المعادن التي تظهر هذا التحول تشمل الحديد والكوبالت, تيتانيوموالقصدير والمنجنيز.
يُشار إلى بلورات العنصر الفلزي نفسه التي توجد في أشكال شبكية مختلفة باسم بلورات متآصلة من الفلز.
الطور: يشير إلى المكونات المتجانسة داخل سبيكة (أو معدن نقي) التي تمتلك نفس التركيب والبنية والخصائص، ويفصلها عن بعضها البعض واجهة بينية.
يمكن تقسيم البنية الطورية في السبائك إلى نوعين بناءً على التفاعل بين العناصر المكونة لها: المحلول الصلب والمركب المعدني.
(1) المحلول الصلب: عندما تتصلب السبيكة السائلة، لا يزال بإمكان العناصر أن تذوب في بعضها البعض لتكوين طور تتشتت فيه ذرات عنصر واحد في شبكة عنصر آخر. تُعرف هذه المرحلة باسم المحلول الصلب.
(2) مركب معدني.
مخطط طور السبيكة، المعروف أيضًا باسم مخطط اتزان السبيكة أو مخطط حالة السبيكة، هو مخطط يوضح العلاقة بين درجة الحرارة والتركيب وحالة السبيكة في ظروف الاتزان. وهو يصور قوانين التغير الهيكلي للسبائك ذات التركيبات المتفاوتة عند تبريدها أو تسخينها ببطء إلى ما لا نهاية.
يُعد مخطط طور السبيكة أداة مهمة لاختيار تركيبة السبيكة المناسبة، وتحليل البنية المجهرية للسبائك، ودراسة خواصها، وتحديد عمليات الصب والتشكيل والمعالجة الحرارية.
(1) مخطط الطور المتجانس: يمثل هذا النوع من المخططات نظام سبيكة حيث يمكن أن يكون المكونان قابلين للامتزاج بشكل لا نهائي في كل من الحالتين السائلة والصلبة. أثناء التصلب، تُشكِّل السبيكة محلولًا صلبًا من الطور السائل، وهي عملية تُعرف باسم التحويل المتجانس.
(2) مخطط الطور سهل الانصهار: في هذا المخطط، يكون مكونان قابلين للامتزاج تمامًا في الحالة السائلة ولديهما تحول سهل الانصهار. يشير التحول سهل الانصهار إلى التبلور المتزامن لمرحلتين صلبتين بتركيبة محددة من مرحلة سائلة موحدة بتركيبة محددة عند درجة حرارة معينة.
(3) مخطط الطور البيروليتيكي: في هذا الرسم البياني، يكون المكونان قابلين للامتزاج بشكل غير محدود في الحالة السائلة ويشكلان محلولاً صلبًا محدودًا في الحالة الصلبة. هناك أيضًا حالة التحول المعماري. يشير التحوُّل المعماري إلى التفاعل بين الطور السائل لمكوِّن معين والطور الصلب لمكوِّن آخر، مما يؤدي إلى تكوين طور صلب جديد عند درجة حرارة ثابتة.

الصلب عبارة عن سبيكة حديد-كربون ذات تركيبة محددة.
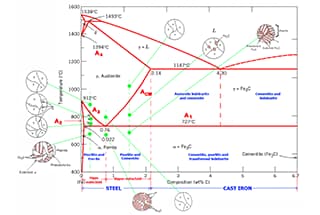
يوضِّح مخطط طور سبيكة الحديد والكربون هياكل التوازن المختلفة لسبائك الحديد والكربون ذات التركيبات المختلفة عند درجات حرارة مختلفة، كما هو موضح في مخطط طور Fe-Fe3C.
من مخطط الطور Fe-Fe3C، يمكننا تحديد درجة الحرارة التي يحدث عندها التحول الطوري في سبيكة حديد-كربون ذات تركيب معين، والمعروفة أيضًا بالنقطة الحرجة.
من خلال تحليل مخطط طور Fe-Fe3C، من الممكن التنبؤ بعملية تحول الطور في مناطق درجات الحرارة المختلفة وبنية التوازن المحتملة عند التبريد إلى درجة حرارة الغرفة.
ارجع إلى النقاط المميزة في مخطط الطور Fe-Fe3C للحصول على وصف لكل نقطة في مخطط طور سبيكة الحديد والكربون، وإلى الخطوط المميزة للحصول على وصف لكل خط.
وفقًا لمخطط طور سبيكة الحديد والكربون، فإن الصلب الكربوني مع محتوى الكربون أقل من 2.11% والحديد الزهر الذي يحتوي على نسبة كربون أكبر من 2.11%.
بناءً على الخصائص الهيكلية، تنقسم سبيكة الحديد والكربون إلى سبع فئات بناءً على محتوى الكربون في مخطط طور سبيكة الحديد والكربون:
(1) حديد نقي صناعي، بمحتوى كربون <0.0218%;
(2) فولاذ سهل الانصهار، بمحتوى كربون 0.77%;
(3) فولاذ Hypoeutectoid، بمحتوى كربوني يتراوح بين 0.0218% إلى 0.77%;
(4) فولاذ فائق الفولاذ، بمحتوى كربوني يتراوح بين 0.77% إلى 2.11%;
(5) حديد الزهر الأبيض سهل الانصهار، بمحتوى كربون 4.30%;
(6) حديد الزهر الأبيض شبه البلوري، بمحتوى كربون يتراوح بين 2.11% إلى 4.30%;
(7) حديد الزهر الأبيض فائق التبلور، بمحتوى كربون يتراوح بين 4.30% إلى 6.69%.
معدن: مادة ذات توصيل حراري وتوصيل كهربائي جيد، وتتميز بمظهرها المعتم وبريقها المعدني. تنخفض توصيلية الفلزات مع زيادة درجة الحرارة، وهي معروفة بقابليتها للسحب والتمدد.
البلورة الفلزية هي مادة صلبة تترتب فيها الذرات في نمط منتظم.
سبيكة: مادة ذات خواص فلزية تتكون من عنصرين أو أكثر، بما في ذلك الفلزات واللافلزات.
تقوية المحلول الصلب: يحدث هذا عندما تشغل ذرات المذاب الفراغات أو الفجوات البينية لشبكة المذيب، مما يتسبب في تشويه الشبكة وزيادة الصلابة والقوة من المحلول الصلب.
مركب: يتم تشكيل بنية صلبة بلورية جديدة ذات خواص فلزية من خلال الجمع بين مكونات السبيكة.
خليط ميكانيكي: تركيبة سبيكة مكونة من بنيتين بلوريتين متميزتين، على الرغم من أنها تظهر ككيان واحد له خواص ميكانيكية مستقلة.
الفريت: محلول صلب خلالي من الكربون في ألفا-في (حديد مكعّب متمركز في الجسم).
أوستنيت: محلول صلب خلالي من الكربون في غاما-في (حديد مكعّب متمركز الوجه).
الأسمنتيت: مركب مستقر (Fe3C) يتكون من اتحاد الكربون والحديد.
بيرلايت: خليط ميكانيكي يتكون من الفريت والأسمنتيت (F + Fe3C، يحتوي على 0.8% كربون).
ليديبوريت خليط ميكانيكي يتكون من الأسمنتيت و الأوستينيت (يحتوي على 4.3% كربون).

تعتبر المعالجة الحرارية للمعادن عملية حاسمة في التصنيع الميكانيكي. وخلافاً لطرق المعالجة الأخرى، لا تغير المعالجة الحرارية الشكل أو التركيب الكيميائي الكلي لقطعة العمل، ولكنها بدلاً من ذلك تعزز أداءها من خلال تعديل بنيتها المجهرية أو التركيب الكيميائي السطحي.
الغرض من المعالجة الحرارية هو تحسين الجودة الداخلية لقطعة الشغل، والتي غالبًا ما تكون غير مرئية للعين المجردة. ولتحقيق الخصائص الميكانيكية والفيزيائية والكيميائية المرغوبة لقطعة الشغل المعدنية، غالبًا ما تكون المعالجة الحرارية ضرورية بالإضافة إلى الاختيار المناسب للمواد ومختلف عمليات التشكيل.
الصلب هو المادة الأكثر استخدامًا في الصناعة الميكانيكية، ويمكن التحكم في بنيته المجهرية من خلال المعالجة الحرارية. ونتيجة لذلك، تعتبر المعالجة الحرارية للصلب جانبًا رئيسيًا من جوانب المعالجة الحرارية للمعادن.
بالإضافة إلى الصلب، يمكن أيضًا استخدام المعالجة الحرارية لتعديل الخصائص الميكانيكية والفيزيائية والكيميائية للألومنيوم والنحاس والمغنيسيوم والتيتانيوم وسبائكها، مما يسمح بتحقيق خصائص خدمة مختلفة.