Was macht Metalle so vielseitig und unverzichtbar für die Technik? In diesem Artikel werden die wesentlichen Grundlagen der Metallkristallisation, -struktur und -umwandlung erläutert. Entdecken Sie, wie Metalle vom flüssigen in den festen Zustand übergehen, die Bedeutung von Kristalldefekten und die faszinierenden Phänomene der Unterkühlung. Wenn Sie diese Prinzipien verstehen, erhalten Sie Einblicke in die Eigenschaften von Metallen und ihre Anwendungen in verschiedenen Branchen.
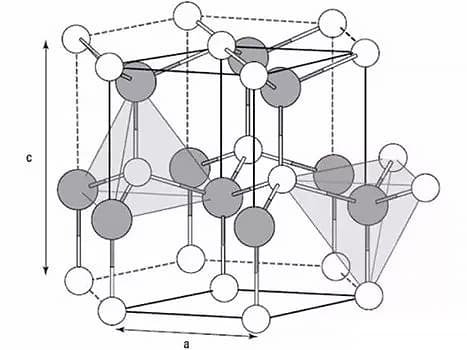
Metalle sind Festkörperkristalle.
Die Kristallstruktur steht im Zusammenhang mit den Eigenschaften, der plastischen Verformung und den Phasenumwandlungen bei der Wärmebehandlung von Metallen.
Die drei häufigsten Gitter in Metallen sind das kubisch-raumzentrierte Gitter, das kubisch-flächenzentrierte Gitter und das dicht gepackte hexagonale Gitter.
Kristalldefekte können aufgrund ihrer geometrischen Form in drei Kategorien eingeteilt werden: Punktdefekte, Liniendefekte und Flächenfehler.
Der Prozess, bei dem ein Metall von einem flüssigen in einen festen (kristallinen) Zustand übergeht, wird als Metallkristallisation bezeichnet.
(1) Abkühlungskurve und Unterkühlungsphänomen
Die Abkühlungskurve ist ein Diagramm, das die Beziehung zwischen Temperatur und Zeit während des Abkühlungsprozesses eines Materials darstellt. Die Abkühlungskurve eines Metallkristalls kann mit Methoden der Thermoanalyse bestimmt werden. Dabei wird das Metall geschmolzen, um eine möglichst gleichmäßige Temperatur zu erreichen, mit einer bestimmten Geschwindigkeit abgekühlt, die Temperaturänderungen über die Zeit aufgezeichnet und die Daten in ein Temperatur-Zeit-Diagramm eingetragen, um die Abkühlungskurve zu erhalten, wie in Abbildung 1 dargestellt.
Die latente Kristallisationswärme, die während der Kristallisation freigesetzt wird, wirkt dem Wärmeverlust des Metalls nach außen entgegen, so dass auf der Abkühlkurve eine horizontale Linie erscheint. Die Temperatur, die dieser Linie entspricht, ist die tatsächliche Kristallisationstemperatur des Metalls.
Experimente zeigen, dass die tatsächliche Kristallisationstemperatur (T1) des Metalls immer niedriger ist als die theoretische Kristallisationstemperatur (T0). Dieses Phänomen wird als Unterkühlung bezeichnet. Unterkühlung ist eine Voraussetzung für das Auftreten von Kristallisationen. Die Differenz zwischen T0 und T1, △T = T0 - T1, wird als Unterkühlungsgrad bezeichnet.
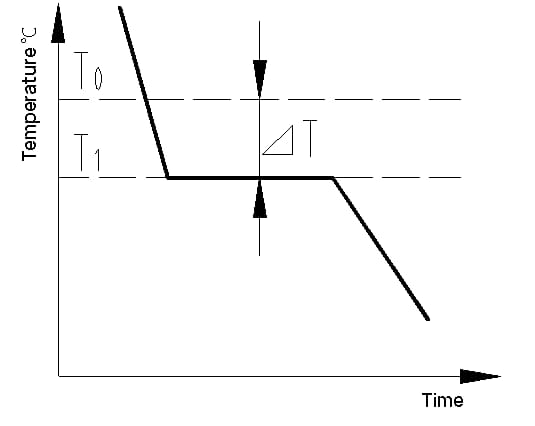
Abb. 1 Abkühlungskurve eines reinen Eisenkristalls
(2) Kristallisationsprozess
Der Prozess der Kristallisation beinhaltet die Bildung und Ausdehnung von Kernen. Dieser Prozess wird als Keimbildung und Wachstum bezeichnet.
Das Phänomen, dass sich ein Metall bei Temperaturänderungen im festen Zustand von einer Gitterstruktur in eine andere umwandelt, wird als isomorphe Umwandlung bezeichnet.
Zu den Metallen, bei denen diese Umwandlung auftritt, gehören Eisen und Kobalt, Titan, Zinn und Mangan.
Kristalle desselben Metallelements, die in verschiedenen Gitterformen vorliegen, werden als allotrope Kristalle des Metalls bezeichnet.
Phase: Bezieht sich auf die einheitlichen Komponenten innerhalb einer Legierung (oder eines reinen Metalls), die die gleiche Zusammensetzung, Struktur und Eigenschaften aufweisen und durch eine Grenzfläche voneinander getrennt sind.
Die Phasenstruktur in Legierungen lässt sich aufgrund der Wechselwirkung zwischen den Bestandteilen in zwei Typen unterteilen: Mischkristall und Metallverbindung.
(1) Feste Lösung: Wenn die flüssige Legierung erstarrt, können sich die Elemente immer noch ineinander auflösen und eine Phase bilden, in der die Atome eines Elements im Gitter eines anderen Elements verteilt sind. Diese Phase wird als Mischkristall bezeichnet.
(2) Metall-Verbindung.
Das Legierungsphasendiagramm, auch bekannt als Legierungsgleichgewichtsdiagramm oder Legierungszustandsdiagramm, ist ein Diagramm, das die Beziehung zwischen Temperatur, Zusammensetzung und Zustand einer Legierung unter Gleichgewichtsbedingungen veranschaulicht. Es zeigt die Gesetze der Strukturveränderung von Legierungen mit unterschiedlichen Zusammensetzungen, wenn sie langsam bis ins Unendliche abgekühlt oder erhitzt werden.
Das Legierungsphasendiagramm ist ein wichtiges Hilfsmittel für die Auswahl der richtigen Legierungszusammensetzung, die Analyse der Mikrostruktur der Legierung, die Untersuchung ihrer Eigenschaften und die Festlegung von Gieß-, Schmiede- und Wärmebehandlungsverfahren.
(1) Homogenes Phasendiagramm: Diese Art von Diagramm stellt ein Legierungssystem dar, bei dem zwei Komponenten sowohl in der flüssigen als auch in der festen Phase unbegrenzt mischbar sein können. Während der Erstarrung bildet die Legierung eine feste Lösung aus der flüssigen Phase, ein Prozess, der als homogene Umwandlung bekannt ist.
(2) Eutektisches Phasendiagramm: In diesem Diagramm sind zwei Komponenten im flüssigen Zustand vollständig mischbar und weisen eine eutektische Umwandlung auf. Unter eutektischer Umwandlung versteht man die gleichzeitige Kristallisation von zwei festen Phasen mit einer bestimmten Zusammensetzung aus einer einheitlichen flüssigen Phase mit einer bestimmten Zusammensetzung bei einer bestimmten Temperatur.
(3) Peritektisches Phasendiagramm: In diesem Diagramm sind zwei Komponenten im flüssigen Zustand unbegrenzt mischbar und bilden im festen Zustand eine endliche feste Lösung. Es gibt auch einen Zustand der peritektischen Umwandlung. Unter peritektischer Umwandlung versteht man die Reaktion zwischen der flüssigen Phase einer bestimmten Komponente und der festen Phase einer anderen Komponente, die zur Bildung einer neuen festen Phase bei konstanter Temperatur führt.

Stahl ist eine Eisen-Kohlenstoff-Legierung mit einem bestimmten Zusammensetzungsbereich.
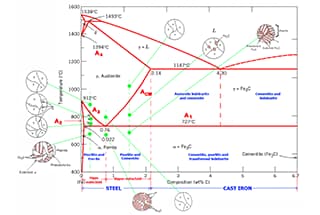
Das Phasendiagramm der Eisen-Kohlenstoff-Legierung veranschaulicht die verschiedenen Gleichgewichtsstrukturen von Eisen-Kohlenstoff-Legierungen mit unterschiedlichen Zusammensetzungen bei verschiedenen Temperaturen, wie sie im Fe-Fe3C-Phasendiagramm dargestellt sind.
Anhand des Fe-Fe3C-Phasendiagramms lässt sich die Temperatur bestimmen, bei der die Phasenumwandlung in einer Eisen-Kohlenstoff-Legierung einer bestimmten Zusammensetzung stattfindet, die auch als kritischer Punkt bezeichnet wird.
Durch die Analyse des Fe-Fe3C-Phasendiagramms ist es möglich, den Phasenumwandlungsprozess in verschiedenen Temperaturbereichen und die potenzielle Gleichgewichtsstruktur beim Abkühlen auf Raumtemperatur vorherzusagen.
Eine Beschreibung der einzelnen Punkte im Phasendiagramm der Eisen-Kohlenstoff-Legierung finden Sie in den charakteristischen Punkten des Fe-Fe3C-Phasendiagramms und eine Beschreibung der einzelnen Linien in den charakteristischen Linien.
Nach dem Phasendiagramm der Eisen-Kohlenstoff-Legierung ist Kohlenstoffstahl mit Kohlenstoffgehalt weniger als 2.11% und Gusseisen mit einem Kohlenstoffgehalt von mehr als 2.11% werden unterschieden.
Auf der Grundlage der strukturellen Merkmale wird die Eisen-Kohlenstoff-Legierung in sieben Kategorien eingeteilt, basierend auf dem Kohlenstoffgehalt im Phasendiagramm der Eisen-Kohlenstoff-Legierung:
(1) Industrielles Reineisen, mit einem Kohlenstoffgehalt < 0,0218%;
(2) Eutektoider Stahl, mit einem Kohlenstoffgehalt von 0,77%;
(3) Untereutektoider Stahl mit einem Kohlenstoffgehalt zwischen 0,0218% und 0,77%;
(4) Übereutektoider Stahl mit einem Kohlenstoffgehalt zwischen 0,77% und 2,11%;
(5) Eutektisches weißes Gusseisen, mit einem Kohlenstoffgehalt von 4.30%;
(6) Subkristallines weißes Gusseisen mit einem Kohlenstoffgehalt zwischen 2,11% und 4,30%;
(7) Super-kristallines weißes Gusseisen mit einem Kohlenstoffgehalt zwischen 4,30% und 6,69%.
Metall: Ein Material mit guter Wärmeleitfähigkeit und elektrischer Leitfähigkeit, das sich durch sein undurchsichtiges Aussehen und seinen metallischen Glanz auszeichnet. Die Leitfähigkeit von Metallen nimmt mit steigender Temperatur ab, und sie sind für ihre Verformbarkeit und Dehnbarkeit bekannt.
Ein Metallkristall ist ein Festkörper, in dem die Atome in einem regelmäßigen Muster angeordnet sind.
Legierung: Ein Stoff mit metallischen Eigenschaften, der aus zwei oder mehr Elementen besteht, einschließlich Metallen und Nichtmetallen.
Verstärkung der festen Lösung: Dies geschieht, wenn gelöste Atome die Räume oder Zwischenräume des Lösungsmittelgitters besetzen, was zu einer Verzerrung des Gitters führt und die Härte und Festigkeit des Mischkristalls.
Verbindung: Durch die Kombination von Legierungsbestandteilen entsteht eine neue kristalline Festkörperstruktur mit metallischen Eigenschaften.
Mechanisches Gemisch: Eine Legierungszusammensetzung, die aus zwei unterschiedlichen Kristallstrukturen besteht, obwohl sie als eine Einheit mit unabhängigen mechanischen Eigenschaften erscheint.
Ferrit: Ein interstitieller Mischkristall aus Kohlenstoff in alpha-Fe (kubisch-raumzentriertes Eisen).
Austenit: Ein interstitieller Mischkristall aus Kohlenstoff in Gamma-Fe (kubisch flächenzentriertes Eisen).
Zementit: Eine stabile Verbindung (Fe3C), die durch die Kombination von Kohlenstoff und Eisen entsteht.
Perlit: Eine mechanische Mischung aus Ferrit und Zementit (F + Fe3C, mit 0,8% Kohlenstoff).
Ledeburit: Ein mechanisches Gemisch, das aus Zementit und Austenit (mit 4,3% Kohlenstoff).

Die Wärmebehandlung von Metallen ist ein wichtiger Prozess in der mechanischen Fertigung. Im Gegensatz zu anderen Verarbeitungsverfahren verändert die Wärmebehandlung nicht die Form oder die chemische Gesamtzusammensetzung des Werkstücks, sondern steigert seine Leistungsfähigkeit durch Veränderung der Mikrostruktur oder der chemischen Zusammensetzung der Oberfläche.
Der Zweck der Wärmebehandlung besteht darin, die innere Qualität des Werkstücks zu verbessern, die mit bloßem Auge oft nicht sichtbar ist. Um die gewünschten mechanischen, physikalischen und chemischen Eigenschaften eines Metallwerkstücks zu erreichen, ist neben der geeigneten Auswahl der Werkstoffe und der verschiedenen Verfahren oft auch eine Wärmebehandlung erforderlich. Formgebungsverfahren.
Stahl ist das am häufigsten verwendete Material in der mechanischen Industrie, und seine Mikrostruktur kann durch Wärmebehandlung gesteuert werden. Folglich ist die Wärmebehandlung von Stahl ein wichtiger Aspekt der Wärmebehandlung von Metallen.
Neben Stahl können durch Wärmebehandlung auch die mechanischen, physikalischen und chemischen Eigenschaften von Aluminium, Kupfer, Magnesium, Titan und deren Legierungen verändert werden, um verschiedene Gebrauchseigenschaften zu erzielen.