Pourquoi certains aciers se plient-ils alors que d'autres se cassent ? Le secret réside dans leur structure cristalline. Cet article explore les différences fascinantes entre les aciers austénitiques, ferritiques, à cémentite et martensitiques. Vous découvrirez comment leurs arrangements atomiques uniques influencent leur résistance, leur flexibilité et leur dureté, offrant des perspectives qui pourraient transformer votre compréhension de la science et de l'ingénierie des matériaux. Préparez-vous à plonger dans le monde microscopique qui façonne les outils et les structures dont nous nous servons tous les jours.
La matière solide dans la nature peut être classée en deux catégories : cristalline et amorphe.
Un cristal est un solide de forme géométrique régulière formé par le processus de cristallisation. Dans un cristal, les atomes ou les molécules sont disposés périodiquement et répétitivement dans l'espace selon une certaine règle.
Un solide amorphe, en revanche, correspond à un cristal dont les atomes ou les molécules sont disposés de manière irrégulière, sans périodicité ni symétrie. Le verre est un exemple de solide amorphe.
Les métaux et alliages solides sont essentiellement des cristaux. La structure cristalline des métaux et des alliages est l'un des facteurs fondamentaux qui déterminent leurs propriétés physiques, chimiques et mécaniques.
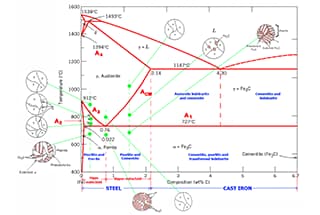
Le fer et l'acier sont des alliages dont les éléments de base sont le fer et le carbone.
Lecture connexe : Acier contre fer
Dans le système Fe-C, lorsque le teneur en carbone est inférieure à 0,02%, le matériau est classé comme fer pur. Si la teneur en carbone dépasse 2,0%, on parle de fonte brute, tandis que la plage comprise entre ces deux limites est classée comme acier.
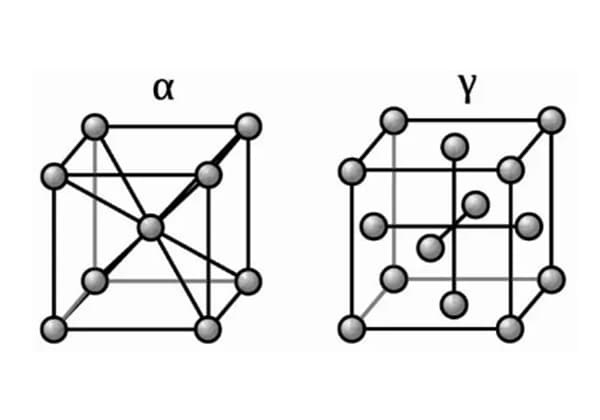
Le fer pur, ou fer forgé, est caractérisé par quatre structures cristallines : α, β, β et δ : α, β, γ et δ. Trois de ces structures, à savoir α, β et δ, présentent des structures centrales cubiques, tandis que la quatrième, c, a une structure centrale cubique.
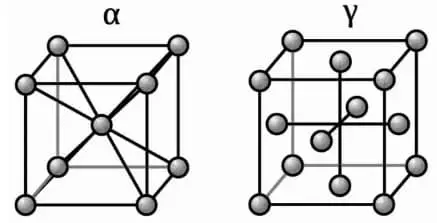
Le fer élémentaire pur cristallise à 1538 ℃ pour former une structure cubique centrale appelée fer δ. En refroidissant à 1394 ℃, il se transforme en une structure cubique à faces centrées appelée fer γ. Un refroidissement supplémentaire jusqu'à 912 ℃ entraîne la formation d'une structure cubique à cœur appelée α-fer.
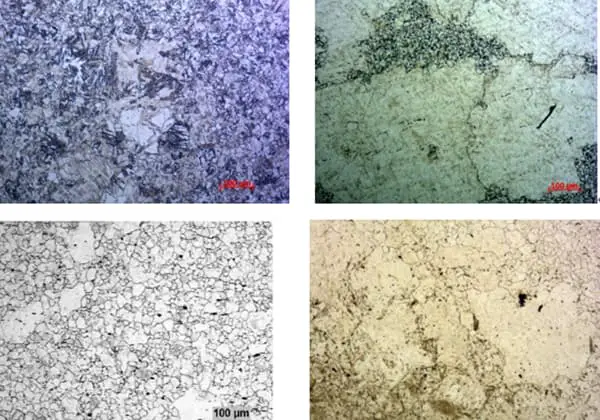
L'acier comporte quatre phases principales : austéniteLes métaux précieux sont la ferrite, la cémentite et la martensite.
Lecture connexe : Fer à béton et fer forgé
Austenite est un composé interstitiel de carbone dans le γ-Fe. Le rapport entre les atomes de Fe et les atomes de C est de 27:1, ce qui signifie qu'un seul atome de C est présent dans toutes les 6-7 cellules cubiques centrées sur la face. La concentration de carbone dissous dans le γ-Fe est de 2.11% à 1148℃ et de 0.77% à 727℃.

Les caractéristiques de l'austénite sont les suivantes la résistance et la dureté sont plus élevés que ceux de la ferrite, tandis que sa plasticité et sa ténacité sont meilleures. En outre, son grain est de forme polygonale et sa limite de grain est plus droite que celle de la ferrite.
La ferrite est une solution solide de carbone dans l'α-Fe, avec une teneur en carbone proche du fer pur, soit environ 0,02%.
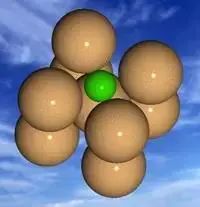
La ferrite possède des caractéristiques similaires à celles du fer pur, notamment une faible résistance et une faible dureté, ainsi qu'une bonne plasticité et une bonne ténacité. Sa microstructure est caractérisée par des grains polygonaux brillants.
La cémentite est un composé de fer et de carbone dans un rapport de 3:1, connu sous le nom de Fe3C. Elle appartient au système cristallin orthogonal et possède une structure cristalline complexe. Chaque cellule de la cémentite est constituée de 12 atomes de Fe et de 4 atomes de C.
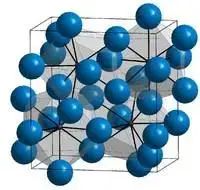
La cémentite se caractérise par une grande dureté, une faible plasticité et une grande ténacité. Ses valeurs de δ et Akk sont proches de zéro et elle présente une grande fragilité.
Lorsque l'acier austénitique est trempé à une température inférieure à 150°C, il se transforme en martensiteLa martensite est extrêmement dure. La martensite peut être considérée comme une solution solide sursaturée composée de 1,6% de carbone dans l'α-Fe, et sa structure cristalline est tétragonale.
Il existe deux types de martensite : la martensite à haute teneur en carbone (martensite lamellaire) et la martensite à faible teneur en carbone (martensite lamellaire).
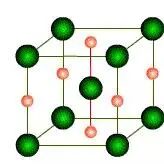
La martensite se caractérise par sa dureté et sa fragilité, sa faible ténacité, sa grande résistance à l'usure et à la corrosion. stress interneet sont susceptibles de se fissurer.
La stabilité des quatre phases varie. La ferrite et la cémentite sont des formes cristallines stables à température ambiante, tandis que l'austénite est stable à haute température.
Lorsque l'acier au carbone est trempé, il obtient principalement de la martensite, qui est une forme cristalline instable. Les aciers d'alliage avec différentes compositions telles que Mn, Ni et Cr peuvent être fabriqués pour différents usages.
Les non-chercheurs de l'industrie de l'acier inoxydable sont principalement exposés à l'austénite, à la ferrite et à la martensite, la cémentite étant plus rarement rencontrée.
L'acier inoxydable est un alliage typique dont les propriétés spéciales sont obtenues en ajoutant des composants d'alliage à la phase de base.